こんにちは、今回は「皮膚筋炎におけるIVIg(免疫グロブリン大量静注療法)の有効性」について取り上げていきたいと思います。
皮膚筋炎は、保健適応となっている免疫抑制薬の選択肢が比較的多くないので、IVIgが効果があるのかすごく期待しています。
〈 用語解説 〉
- DM:皮膚筋炎
- IVIg;免疫グロブリン大量静注療法
皮膚筋炎におけるIVIg(免疫グロブリン大量静注療法)の有効性について

皮膚筋炎における免疫グロブリン大量静注療法(IVIg)の有効性を検証した、ランダム化比較試験【ProDERM試験】についての報告が、2022年6月に臨床系の有名誌 『 New England Journal of Medicine1) 』に掲載されました。
今回は、こちらをご紹介します。
IVIgの作用機序は?
(画像引用:https://chisatp.net/archives/10976580.html)
大量ガンマグロブリン療法(IVIg)は比較的安全に施行でき、免疫不全や重症感染症、膠原病といった自己免疫疾患などに使用されている治療法です。
作用機序は多くにわたりますが、Lünemannらのレビューでは2)、
- 細胞表面に発現するFasに結合し、細胞間のシグナル伝達を抑える
- サイトカイン、自己抗体を中和する
- Fc受容体を介した細胞の活性化を抑制する
- 胎児性Fc受容体による抗体のリサイクルを抑制する
といった4つの機序が推定されています。
皮膚筋炎患者におけるIVIgの作用機序は十分に解明されていませんが、
〈 皮膚筋炎患者におけるIVIgの作用機序 〉

- 補体消費の阻害と膜攻撃複合体の形成の阻害の関与の可能性3,4)(皮膚筋炎においてC3の活性化は、筋内膜毛細血管への膜攻撃複合体の形成と沈着、およびそれに続く毛細血管の破壊をもたらして微小血管障害を引き起こす5-8))。
- IVIgが皮膚筋炎においてサイトカインやケモカインのダウンレギュレーションや遺伝子発現の修飾をもたらす可能性3,4)。
が考えられています。
本邦の皮膚筋炎におけるIVIgの適応
日本では、多発性筋炎・皮膚筋炎における、ステロイドが効果不十分な場合の筋力低下の改善において保健適応されています。
方法 Methods

まずは、ProDERM試験の概要についてです。
- 試験デザイン:前向き第3相二重盲検、並行群間、ランダム化比較試験
- 地域:欧米36施設
- 対象:
- Bohan & Peterの診断基準を満たした活動性皮膚筋炎患者
- 18歳〜80歳
- 方法:
- 患者は1:1の割合で、体重1kgあたり2.0gのIVIgまたはプラセボを4週おきに16週間投与されるように割り付けられた。
- プラセボの患者さん、およびIVIG投与中に臨床的な悪化が確認されなかった患者さんは、さらに24週間の非盲検延長試験に入り、いずれの群もIVIg(2g/kg)を4週毎に投与された。
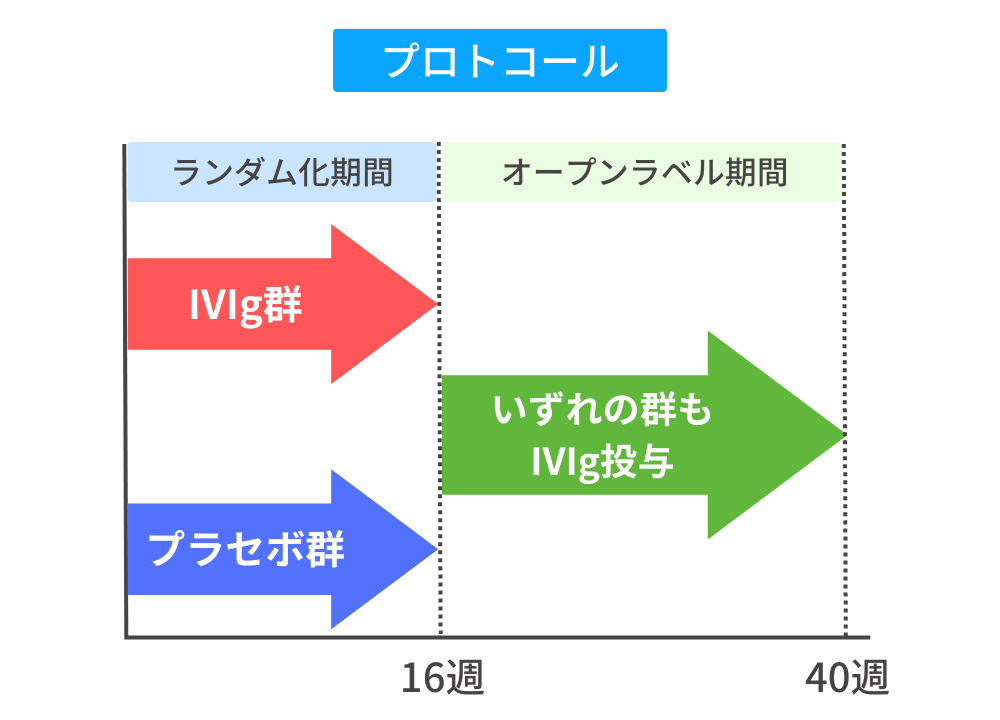

- 主要エンドポイント:奏功と定義。具体的には、16週目のTotal Improvement Score(TIS:筋炎の総合改善スコア)が20以上(少なくとも最小限の改善を示す)であり、16週目まで悪化が確認されないこと。
- 副次エンドポイント:中等度以上の改善(TIS 40 以上),大きな改善(TIS 60 以上),皮膚筋炎のCDASIスコア(皮膚筋炎の病変範囲と重症度)の変化など
- その他:
- 試験登録時のプレドニゾロン換算で1日20mgを最大許容量とし、試験のランダム化比較試験中は登録時の投与量を維持した。
- ステロイドに加えて許可された併用療法は、最大2種類の免疫抑制剤(メトトレキサート、アザチオプリン、ミコフェノール酸モフェチル、スルファサラジン、レフルノミド、タクロリムス、サイクロスポリン、ヒドロキシクロロキン)。
● TIS(Total Improvement Score)とは?

TIS(筋炎の総合改善スコア)は、筋炎の活動性に関する6つの主要評価項目の経時的変化を反映した加重複合スコアのことです。
スコアは0から100まであり、スコアが高いほど改善が大きいことを示します。
ベースラインの特徴

ベースラインの特徴を見ていきましょう。
| 合計 = 95 | IVIg n=47 | プラセボ n=48 |
| 年齢(中央値) | 55 (22-77) | 51.5 (22-79) |
| 女性 | 36 (77%) | 35 (73%) |
| 罹患期間(中央値) | ||
| 皮膚筋炎の分類 (Bohan&Peterの基準) | ||
| Definite | 34 (72%) | 33 (69%) |
| Probable | 13 (28%) | 15 (31%) |
| 皮膚筋炎の活動性 | ||
| 軽症 | 11 (23%) | 15 (31%) |
| 中等症 | 29 (62%) | 27 (56%) |
| 重症 | 7 (15%) | 6 (12%) |
| 併用薬 | ||
| 経口ステロイド | 40 (85%) | 44 (92%) |
| 非ステロイド薬 | 31 (66%) | 34 (71%) |
結果 Results

それでは、結果を見ていきましょう。
16週後の有効性はどうでしたか?【主要エンドポイント】

IVIgの16週後の活動性皮膚筋炎に対しての効果はどうだったのでしょうか?
16週時点での20以上のTI(総改善)スコアの奏功は、IVIg群では79%( 37/47 )、プラセボ群では44%( 21/48 )で、IVIg群が有意に高い改善を認めました。
| IVIg | プラセボ | |
| 16週目の20以上の TISスコアの改善(%) | 79 % ( 37/47 ) | 44 % ( 21/48 ) |
| 調整後差: 35 % 95%CI:16.7~53.2 | P<0.001 |
また、16週時点でのMeanTI(総改善)スコアの点数は、IVIg群は 48.4、プラセボ群は 21.6で、差は26.8でした(下図)。
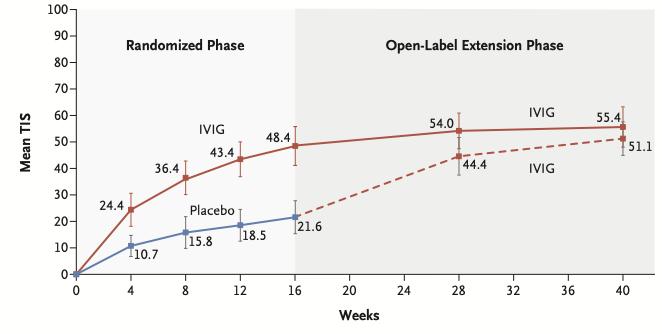
〈 図:16週、40時点でのTI(総改善)スコア 〉

副次エンドポイント
続いて、副次エンドポイントです。
TISスコアの中等度以上や大きな改善はどうでしたか?

16週時点でのTI(総改善)スコア 40以上の中等度以上の改善は、IVIg群で68% ( 32/47 ) 、プラセボ群で23% ( 11/48 )に認められました。
また、16週時点でのTI(総改善)スコア 60以上の大きな改善は、 IVIg群で 32 % ( 15/47 ) 、プラセボ群で8 % ( 4/48 ) に認められました。
しかし、副次エンドポイント解析における群間差の95%信頼区間の幅は、複数の比較で調整されておらず、これらのデータから明確な結論は導き出されていません。
| IVIg | プラセボ | |
| 16週目の40以上の TISスコアの改善(%) | 68 % (32/47) | 23 % (11/48) |
| 調整後差: 45% 95%CI:27 ~ 63 | ||
| 16週目の60以上の TISスコアの改善(%) | 32 % (32/47) | 8 % (4/48) |
| 調整後差: 24% 95%CI:8 ~ 39 |
CDASI(皮膚筋炎の病変範囲と重症度)スコアはどうでしたか?
CDASIスコアのベースラインからの平均変化は、一次解析の結果と概ね同じで、IVIgの方がより改善させる傾向にありました(こちらも有意差までは出せていません)。
| IVIg | プラセボ | |
| 総活動性スコアにおける平均変化 | ||
| ベースラインから16週 (95%CI) | -9.4 (-12.5 to -6.2) | -1.2 (13.3 to 1.0) |
| 差 -8.0 | 95%CI: -11.5 to -4.6 | |
| 16週から40週 (95%CI) | -1.8 (-3.3 to -0.3) | -8.5 (-12.5 to -4.5) |
| 総活ダメージスコアにおける平均変化 | ||
| ベースラインから16週 (95%CI) | -0.7 (-1.2 to -0.1) | -0.02 (-0.26 to 0.21) |
| 差 -0.6 | 95%CI: -1.1 to -0.1 | |
| 16週から40週 (95%CI) | 0.3 (-0.5 to 1.0) | -0.2 (-0.6 to 0.1) |

筋力の改善はどうでしたか?
筋力については、MMT-8スコア(徒手筋力検査のスコア)を参照します。
16週時点で、MMT-8スコアの平均変化は、 IVIg群で14.4(10-18.8)、プラセボ群で3.2 (0.3-6.1) で、IVIg群の方がより筋力の改善を認める傾向にありました(こちらも有意差までは出せていません)。
| IVIg | プラセボ | |
| MMT-8スコアの平均変化 | ||
| ベースラインから16週 (95%CI) | 14.4 (10 to 18.8) | 3.2 (0.3 to 6.1) |
| 差 8.6 | 95%CI: 4.4 to 12.8 | |
| ベースラインから40週 (95%CI) | 20.1 (15 to 25.2) | 12 (9.4 to 14.6) |
40週時点での有効性はどうでしたか?
16週から40週の間は、IVIg群とプラセボ群はいずれも、IVIg 2g/kgを4週に1回 計6回投与されていることに注意ください。
40週時点で、両群の約60%の患者に中等度以上の改善が認められ、両群の30%以上の患者に大きな改善が認められた 。
| IVIg | プラセボ | |
| 40週目の20以上のTISスコアの改善(%) | 71 % | 70 % |
| 40週目の40以上のTISスコアの改善(%) | 58 % | 61 % |
| 40週目の60以上のTISスコアの改善(%) | 38 % | 30 % |

安全性はどうでしたか?

最後に安全性についてです。
ランダム化比較対照試験では、IVIg群の 58%(30/52) に計113件、プラセボ群の 23% (11/48) に計38件の何らかの有害事象が認められました。
オープンラベル期間を含む試験全体では、全患者の65%(62/95)に計282件の有害事象が認められました。
IVIg投与で観察されたもので最も多かったのは、頭痛 (42%) 、発熱 (19%) 、吐き気 (16%) でした。
IVIgには血栓塞栓症のリスクがあること9-12)が言われていますが、
本試験での血栓塞栓イベントは、試験全体で、IVIgを受けた6人の患者で8件認めました。
血栓塞栓症には特に気をつけないといけませんね。
| IVIg | プラセボ | 全期間 IVIg | |
| 何らかの有害事象の発生 | 58 % ( 113件 ) | 23 % ( 38件 ) | 65 % ( 282件 ) |
| 頭痛 | 37 | 6 | 42 |
| 発熱 | 19 | 6 | 19 |
| 吐き気 | 12 | 4 | 16 |
| 嘔吐 | 6 | 0 | 8 |
| 悪寒 | 6 | 2 | 7 |
| 筋肉痛 | 6 | 0 | 7 |
| 高血圧 | 6 | 6 | 6 |
| 深部静脈血栓症 | 0 | 0 | 1※ |
| 肺塞栓症 | 0 | 0 | 1※ |
| 脳血管障害 | 0 | 0 | 1 |
| 脳梗塞 | 0 | 0 | 1 |
| 感覚鈍麻 | 0 | 0 | 1 |
| 肺塞栓症 | 0 | 0 | 1 |
※ 深部静脈血栓症と肺塞栓症は、1名の患者において2つの事象が同時に発生したため、1つの血栓塞栓症の有害事象としてカウント。
今回のまとめ
- IVIg(大量グロブリン静注療法)は、活動性皮膚筋炎患者の16週時の20%以上のTI(総改善)スコアをプラセボと比較して有意に改善させた。
- また、16週時の中等度以上または大きな改善を示したのも、IVIg群の方が高かった。
- 筋力や皮疹などの結果も概ね同様であった。
- IVIgは、頭痛、発熱、吐き気や血栓塞栓症といった有害事象と関連していた。
本研究の限界(limitation)
- ランダム化比較対照試験の期間は16週間と短く、若年性皮膚筋炎、腫瘍関連皮膚筋炎、または無筋症性皮膚筋炎の患者は除外されたこと。
- 筋炎の自己抗体は系統的に収集されておらず、自己抗体のサブセットによってIVIgの効果を評価できていないこと。
- プラセボ群の奏効率は高く、これは最小の改善を達成するために設定された閾値の低さ、背景の免疫抑制、疾患活動性のPhGAやPtGAなどのいくつかのエンドポイント指標の主観的な性質が原因である可能性があること。

〈参考〉
- 1) Rohit Aggarwal, et al. N Engl J Med 2022;387:1264-78.
- 2) Lünemann JD, et al. Nat Rev Neurol. 2015; 11: 80-89.
- 3) Dalakas MC, et al. J Clin Immunol 2014;34:S120-S126.
- 4) Quick A, et al. Curr Rheumatol Rep 2011;13:192-8.
- 5) Basta M, et al. Nat Med 2003;9:431-8.
- 6) Basta M, et al. J Clin Invest 1994;94:1729-35.
- 7) Emslie-Smith AM, et al. Ann Neurol 1990;27:343-56.
- 8) Kissel JT, et al. N Engl J Med 1986;314:329-34.
- 9) Paran D, et al. Blood Coagul Fibrinolysis 2005;16:313-8.
- 10) Marie I, Maurey G, et al. Br J Dermatol 2006;155: 714-21.
- 11) Caress JB, et al. Expert Opin Drug Saf 2010;9: 971-9.
- 12) Kapoor M, et al. J Neurol Neurosurg Psychiatry 2022;93: 876-85.

今回はここまでです。最後までお読み頂きありがとうございました。ご参考になりましたら幸いです。
Twitterでのいいねやフォローをして頂けますと励みになりますので、ぜひよろしくお願いします!
リンク

現役医師が作ったヘルスケアプリ『 マイカル 』2025年7月リリース!!
iPhone版のURLとQRコード👇
https://apps.apple.com/jp/app/%E3%83%9E%E3%82%A4%E3%82%AB%E3%83%AB/id6748717829

Android版のURLとQRコード👇
https://play.google.com/store/apps/details?id=com.mycal.medlife

MedLifeチャンネル 〜役立つ医療情報を動画で紹介〜
※個人個人で症状の違いがあるため、詳細な治療などにつきましては直接医療機関へお問い合わせください。